再生医療は、傷害を受けた組織を細胞や組織の再生能力により修復したり、特定の細胞が持つ機能を活用して疾患を治癒したりする医療のことをいいます。
再生医療が医療関係者ではない一般の人々の間でも広く認識されるきっかけになった出来事は、2012年(平成24年)のノーベル医学生理学賞が山中伸弥教授の人工多能性幹細胞(iPS細胞)の研究に授与されたことでしょう。多能性幹細胞は、その高い増殖能力及びあらゆる種類の細胞に分化し得る能力から再生医療に応用されることを大いに期待されました。
このような背景から、早くも2013年(平成25年)4月には「再生医療を国民が迅速かつ安全に受けられるようにするための施策の総合的な推進に関する法律」が成立して5月に同法が施行され、次いで同年の11月には「再生医療等の安全性の確保等に関する法律(再生医療等安全性確保法)」が成立し、2014年(平成26年)に施行されました。同時に薬事法が改正・施行されました。この改正薬事法は、改称され、その正式名称を略して「医薬品医療機器等法」又は「薬機法」と呼ばれています。薬機法には再生医療等製品の承認・許可に関する規定があります。このようにして再生医療の実施を法的に支援する制度が整いました。
この記事は、再生医療の提供を考えているクリニックの方々に再生医療提供の規制を理解してもらうため、再生医療等安全性確保法等の内容を紹介します。
再生医療等安全性確保法の紹介
再生医療等安全性確保法の構成
再生医療等安全性確保法の構成は次のようになっています。
- 第一章 総則(第1条、第2条)
- 第二章 再生医療等の提供
- 第一節 再生医療等提供基準(第3条)
- 第二節 再生医療等の提供の開始、変更及び中止の手続
- 第一款 通則(第4条~第6条)
- 第二款 第一種再生医療等の提供に関する特則(第7条~第10条)
- 第三款 第二種再生医療等の提供に関する特則(第11条)
- 第三節 再生医療等の適正な提供に関する措置(第12条~第25条)
- 第三章 認定再生医療等委員会(第26条~第34条)
- 第四章 特定細胞加工物の製造(第35条~第54条)
- 第五章 雑則(第55条~第58条)
- 第六章 罰則(第59条~第64条)
再生医療等安全性確保法において第4条~第11条は再生医療等を提供する場合に医療機関が行う手続を規定しています。これらの条項において規定されている手続には事前の手続も含まれます。第12条~第25条は医療機関が再生医療等の提供を適正に行うための措置を規定しています。
第26条~第34条は認定再生医療等委員会を規定しています。認定再生医療等委員会については後に詳しく説明します。
第35条~第54条は特定細胞加工物の製造業者が再生医療等の提供者の委託を受けて特定細胞加工物を製造する場合にその事業者が行う手続を規定しています。
再生医療等安全性確保法は、再生医療等の提供に係る手続又は再生医療等に使用する特定細胞加工物の製造に係る手続を怠った場合に再生医療等提供者又は特定細胞加工物製造事業者に適用される罰則を含み、これらの罰則は第59条~第64条に規定されています。
再生医療等安全性確保法施行規則の構成
再生医療等安全性確保法の各規定の実現に必要な詳細が、再生医療等安全性確保法施行規則に定められています。再生医療等安全性確保法施行規則の構成は次のようになっています。
- 第一章 総則(第1条~第3条)
- 第二章 再生医療等の提供
- 第一節 再生医療等提供基準(第4条~第26条の13)
- 第二節 再生医療等提供計画(第27条~第31条の3)
- 第三節 再生医療等の適正な提供に関する措置(第32条~第41条)
- 第三章 認定再生医療等委員会(第42条~第71条の2)
- 第四章 特定細胞加工物の製造(第72条~第112条)
- 第五章 監督(第113条~第117条)
- 第六章 雑則(第118条~第122条)
再生医療等安全性確保法の内容の説明
再生医療は未だ研究段階のものも多く、自由診療として実施される場合がほとんどであるのが現状です。再生医療の施術を受ける患者が享受するベネフィットとリスクを鑑みて、再生医療等安全性確保法が制定されました。
本記事は、認定再生医療等委員会及び特定細胞加工物の製造に係る規定を除く、再生医療等安全性確保法及び再生医療等安全性確保法施行規則の規定を紹介します。認定再生医療等委員会及び特定細胞加工物の製造に係る規定については後続の記事において紹介する予定です。
第一章 総則
再生医療等安全性確保法は、再生医療等に用いられる再生医療等技術の安全性の確保及び生命倫理への配慮に関する措置その他再生医療等提供者が講ずべき措置を明示し、特定細胞加工物の製造の許可等を定めることにより、再生医療等の迅速かつ安全な提供及び普及の促進を図り、もって医療の質及び保健衛生の向上に寄与することを目的としています(法第1条)。
用語の定義(法第2条)
自由診療: 治療として国の承認を受けるための要件を満たしておらず、公的には有効性等が確認されていないために公的医療保険が適用されない診療
再生医療等: 再生医療等技術を用いて行われる医療
再生医療等技術: 人の身体の構造若しくは機能の再建、修復、若しくは形成、又は人の疾病の治療若しくは予防に用いられることが目的とされている医療技術であって、細胞加工物(再生医療等製品のみを当該製品の薬機法上の承認の内容に従って用いるものを除く)を用いるもののうち、政令で定めるもの
特定細胞加工物: 人又は動物の細胞に培養その他加工を施した細胞加工物のうち、再生医療等に用いられる細胞加工物であって、再生医療等製品に該当しないもの
(「加工」とは、細胞や組織の人為的な増殖、分化、細胞株化、及び活性化等を目的とした薬剤処理、生物学的特性改変、非細胞成分との組合せ又は遺伝子工学的改変等を施すことであり、細胞や組織の分離、組織の細断、特定細胞の単離(薬剤等による生物学的・化学的処理による単離を除く)、抗生物質処理、洗浄、ガンマ線等による滅菌、冷凍又は解凍ではないものをいいます)
再生医療等安全性確保法で規定される「再生医療等」は、上の用語の定義からわかるように、①人の身体の構造若しくは機能の再建、修復、若しくは形成、又は人の疾病の治療若しくは予防を目的としていること、及び②細胞加工物を用いることという二つの要件を満たす医療をいいます。
輸血、造血幹細胞移植、及び生殖細胞を用いる医療技術は、政令により、再生医療等安全性確保法で規定される「再生医療等技術」に該当しないことになっています。但し、これらの施術であっても「再生医療等」に該当する場合もあるので注意が必要です。厚生労働大臣は、この政令の制定又は改廃の立案をしようとするときは、あらかじめ、厚生科学審議会の意見を聴取することになっています(法第55条第1項)。
造血幹細胞移植の場合、移植に用いる造血幹細胞の適切な提供の推進に関する法律(造血幹細胞移植法)が再生医療等安全性確保法に先んじて2012年(平成24年)に成立しており、造血幹細胞移植法制定時に一定の効果があり、広く行われているとの評価を受けている医療技術を用いた造血幹細胞の移植は、造血幹細胞移植法上の造血幹細胞移植に当たるため、再生医療等安全性確保法の対象になりません。
再生医療等安全性確保法第2条の定義によると、再生医療等は第一種再生医療等、第二種再生医療等、及び第三種再生医療等に分類され、それらの再生医療等は各々第一種再生医療等技術、第二種再生医療等技術、及び第三種再生医療等技術を用いて行われる再生医療等をいいます。
これらの再生医療等技術は、それらの医療技術の潜在的なリスクに応じて次のように分類されています。
第一種再生医療等技術: 人の生命及び健康に与える影響が明らかでない又は相当の注意をしても人の生命及び健康に重大な影響を与える可能性がある再生医療等医療技術であって厚生労働省令で定めるもの
第二種再生医療等技術: 相当の注意をしても人の生命及び健康に影響を与える可能性がある再生医療等医療技術であって厚生労働省令で定めるもの
第三種再生医療等技術: 第一種再生医療等技術でも第二種再生医療等技術でもない再生医療等技術
これらの第一種再生医療等技術及び第二種再生医療等技術に係る厚生労働省令は、厚生科学審議会の意見を聴取して厚生労働大臣によって制定又は改廃されるものですが、厚生労働大臣は、その際には、あらかじめ、厚生科学審議会の意見を聴取することになっています(法第55条第2項)。
再生医療等安全性確保法施行規則では第一種再生医療等技術及び第二種再生医療等技術は次のように具体的に掲げられています。
第一種再生医療等技術(施行規則第2条)
- 人の胚性幹細胞、人工多能性幹細胞又は人工多能性幹細胞様細胞に培養その他の加工を施したものを用いる医療技術
- 遺伝子を導入若しくは改変する操作を行った細胞又は当該細胞に培養その他の加工を施したものを用いる医療技術(前号に掲げるものを除く)
- 動物の細胞に培養その他の加工を施したものを用いる医療技術(前二号に掲げるものを除く)
- 投与を受ける者以外の人の細胞に培養その他の加工を施したものを用いる医療技術(前三号に掲げるものを除く)
第一種再生医療等技術のうち第1号、第3号、及び第4号は基本的に患者自身以外の細胞を利用する技術であるといえます。
第二種再生医療等技術(施行規則第3条)
- 培養した幹細胞又は当該細胞に培養その他の加工を施したものを用いる医療技術
- 培養した細胞又は当該細胞に培養その他の加工を施したものを用いる医療技術のうち人の身体の構造又は機能の再建、修復又は形成を目的とする医療技術(前号に掲げるものを除く)
- 細胞の相同利用ではない医療技術(前二号に掲げるものを除く)
第二種再生医療等技術で使用される細胞及び幹細胞は、患者自身の細胞又は幹細胞になります。第2号の医療技術のポイントは、使用される「培養した細胞」が幹細胞ではないことです。「細胞の相同利用」とは、患者の再生医療等の対象となる部位の細胞と同様の機能を持つ細胞をその部位に投与することをいいます。
以上の規定から、第三種再生医療等技術は次のように考えられます。
第三種再生医療等技術
- 培養その他の加工を施さずにヒト幹細胞をそのまま用いる医療技術であって、細胞の相同利用である医療技術
- 培養その他の加工を施さずにヒト細胞(幹細胞を除く)をそのまま用いる医療技術であって、細胞の相同利用である医療技術のうち人の身体の構造又は機能の再建、修復又は形成を目的とする医療技術
- 培養したヒト細胞(幹細胞を除く)又は当該細胞に培養その他の加工を施したものを用いる医療技術であって、細胞の相同利用である医療技術(人の身体の構造又は機能の再建、修復又は形成を目的としないもの)
ここで第3号の第2号との違いは、培養その他の加工を施した細胞(幹細胞を除く)を使用することであり、それは人の身体の構造又は機能の再建、修復又は形成を目的としないのなら培養細胞の使用が許されることを表しています。
第二章 再生医療等の提供
第一節 再生医療等提供基準
再生医療等安全性確保法は、厚生労働大臣が、厚生労働省令で、再生医療等の提供に関する基準(「再生医療等提供基準」)を定めるとしており(法第3条第1項)、再生医療等は、再生医療等提供基準に従って提供されるとしています(法第3条第3項)。
再生医療等提供基準(法第3条第2項)
- 再生医療等を提供する病院又は診療所が有すべき人員及び構造設備その他の施設に関する事項
- 再生医療等に用いる細胞の入手の方法並びに特定細胞加工物の製造及び品質管理の方法に関する事項
- 前二号にあげるものの他、再生医療等技術の安全性の確保等に関する措置に関する事項
- 再生医療等に用いる細胞を提供する者及び再生医療等(研究として行われる場合その他の厚生労働省令で定める場合に係るものに限定)を受ける者に対する健康被害の補償の方法に関する事項
- その他再生医療等の提供に関し必要な事項
第4号の「その他の厚生労働省令で定める場合」は、現在のところ「研究として行われる場合」になっています。
この再生医療等提供基準は、厚生労働大臣によって制定又は変更されるものですが、厚生労働大臣は、その際には、あらかじめ、厚生科学審議会の意見を聴取することになっています(法第55条第3項)。
再生医療等を提供しようとしている医療機関は、法第3条第3項の規定に従い、以下の再生医療等提供基準を満たす必要があります。
法第3条第2項第一号の基準(人員及び構造設備等に関する事項)
法第3条は、第1項において、厚生労働大臣が再生医療等提供基準を定めるとしており、同条第2項において、厚生労働大臣が定めるべき種々の再生医療等提供基準を挙げています。これらの再生医療等提供基準は、具体的には、再生医療等安全性確保法施行規則で定められています。
再生医療等を提供する医療機関の人的基準は、次のようになっています。
第一種再生医療等又は第二種再生医療等の提供を行う医療機関は、その第一種再生医療等又は第二種再生医療等に関する業務の実施を統括するため、当該業務に係る責任者(「実施責任者」)を置く必要があります(施行規則第5条第1項)。
実施責任者は、医師又は歯科医師であって、実施する第一種再生医療等又は第二種再生医療等の対象となる疾患及び当該疾患に関連する分野について、十分な科学的知見並びに医療に関する経験及び知識を有している必要があり、研究として再生医療等を行う場合には、研究に関する倫理に配慮して当該研究を適正に実施するための十分な教育及び訓練を受けていなければなりません(施行規則第5条第2項)。
再生医療等を提供しようとしている医療機関の構造設備的基準は、次のようになっています。
第一種再生医療等又は第二種再生医療等の提供を行う医療機関は、その医療機関において再生医療等を受ける者に対して救急医療を行うために必要な施設又は設備を有している必要があります。ただし、他の医療機関と連携することにより、その者に対して救急医療を行うために必要な体制があらかじめ確保されている場合には、この限りではありません(施行規則第6条)。
法第3条第2項第二号の基準(細胞の入手の方法並びに特定細胞加工物の製造及び品質管理の方法に関する事項)
再生医療等に用いる細胞の入手の方法並びに特定細胞加工物の製造及び品質管理の方法に関する基準(法第3条第2項第二号)は、次のとおりです。
再生医療等を行う医師又は歯科医師は、再生医療等に用いる細胞が、次に掲げる要件を満たすことを確認し、必要に応じ検査等を行い、当該細胞を再生医療等に用いることが適切であることを確認しなければなりません(施行規則第7条)。
再生医療等に用いる細胞の要件(施行規則第7条)
- 次に掲げる要件を満たした医療機関等において細胞の提供(細胞提供者からの細胞の提供に限る)又は動物の細胞の採取が行われたこと。
- イ 適切に細胞の提供を受け又は動物の細胞の採取をし、当該細胞の保管に当たり必要な管理を行っていること
- ロ 細胞の提供を受けること又は動物の細胞の採取をすること並びに当該細胞の保管に関する十分な知識及び技術を有する者を有していること
- 細胞の提供を受ける際に、細胞提供者の健康状態、年齢その他の事情を考慮した上で、当該細胞提供者の選定がなされたこと。
- 細胞の提供を受ける際に、細胞提供者が細胞の提供を行うのに十分な適格性を有するかどうかの判定をするために、利用の目的に応じて、既往歴の確認、診察、検査等を行ったこと。
- 細胞の提供を受けた後に、感染症の感染後、検査をしても感染を証明できない期間があることを勘案し、検査方法、検査項目等に応じて、可能な範囲で、適切な時期に再検査を実施していること。
- 死亡した者から細胞を採取する場合にあっては、礼意を失わないように注意し、遺族に対して、細胞の使途その他細胞の採取に関し必要な事項について、できる限り平易な表現を用い、文書により適切な説明を行い、文書により同意を得ていること。
- 細胞の提供を受ける際に、細胞提供者に対し、原則として、次に掲げる事項について、できる限り平易な表現を用い、文書により適切な説明を行い、文書により同意を得ていること。
- 細胞提供者の代諾者に対する説明及び同意については前号の規定を準用する。
- 細胞の提供を受ける際に、代諾者の同意を得た場合には、代諾者の同意に関する記録及び代諾者と細胞提供者との関係についての記録が作成されていること。
- 細胞提供者又は代諾者が当該細胞を再生医療等に用いることについて同意した場合であって、当該細胞に培養その他の加工が行われるまでの間について、当該細胞提供者又は代諾者が同意を撤回することができる機会が確保されていること。
- 人の受精胚の提供を受ける場合にあっては、当該細胞の提供に係る同意があった後、少なくとも30日間は人の胚性幹細胞の樹立に供することなく医療機関において当該細胞を保管し、細胞提供者に対し、当該者が同意を撤回することができる機会が確保されていること。
- 人の受精胚の提供を受ける場合にあっては、次に掲げる要件を満たしたものであること。
- イ 生殖補助医療に用いる目的で作成された受精胚であって、当面当該目的に用いる予定がないもののうち、当該受精胚を滅失させることについて提供者の意思が確認できたものであること
- ロ 凍結保管がされているものであること
- ハ 凍結保管されている期間を除き、受精後14日以内のものであること
- ニ その他人の胚性幹細胞の樹立の適正な実施のために必要な手続を経たものであること
- 細胞の提供が無償で行われたこと。ただし、細胞の提供に際し発生した交通費その他の実費に相当するものについてはこの限りでない。
- 細胞の提供を受ける際に、その過程における微生物等による汚染を防ぐために必要な措置が講じられていること。
- 細胞の提供を受けた当該細胞について、微生物等による汚染及び微生物等の存在に関する適切な検査を行い、これらが検出されないことを、必要に応じ、確認したものであること。
- 細胞の採取を行う場合にあっては、細胞の採取を優先し、医学的処置、手術及びその他の治療の方針を変更することにより採取された細胞でないこと。
- 動物の細胞を用いる場合にあっては、細胞の採取に当たり、次に掲げる要件を満たしていること。
- イ 細胞を採取される動物の状態その他の事情を考慮した上で、当該動物の選定がなされたこと
- ロ 細胞の採取の際に、当該動物が細胞を採取されるにつき十分な適格性を有するかどうかの判定をするために、利用の目的に応じて既往歴の確認、診察、検査等を行ったこと
- ハ 動物の細胞の採取の過程における微生物等における汚染を防ぐために必要な措置が講じられていること
上の第六号の説明事項の内容は、次のとおりです。
細胞提供者に説明し、同意を取り付ける事項(施行規則第7条第六号)
- イ 提供する再生医療等の名称及び当該再生医療等の提供について厚生労働大臣に再生医療等提供計画(法第4条第1項に規定する再生医療等提供計画をいう)を提出している旨
- ロ 細胞の提供を受ける医療機関等の名称及び細胞の採取を行う医師又は歯科医師の氏名
- ハ 当該細胞の使途
- ニ 細胞提供者として選定された理由
- ホ 当該細胞の提供により予期される利益及び不利益
- ヘ 細胞提供者となることは任意であること。
- ト 同意の撤回に関する事項
- チ 当該細胞の提供をしないこと又は同意を撤回することにより不利益な取扱いを受けないこと。
- リ 研究に関する情報公開の方法(研究として再生医療等を行う場合に限る)
- ヌ 細胞提供者の個人情報(法第15条に規定する個人情報をいう)の保護に関する事項
- ル 試料等(人体から取得された試料及び再生医療等に用いる情報をいう)の保管及び廃棄の方法
- ヲ 研究に対する施行規則第8条の8第1項各号に規定する関与に関する状況(研究として再生医療等を行う場合に限る)
- ワ 当該細胞を用いる再生医療等に係る特許権、著作権その他の財産権又は経済的利益の帰属に関する事項
- カ 苦情及び問合せへの対応に関する体制
- ヨ 当該細胞の提供に係る費用に関する事項
- タ 当該細胞の提供による健康被害に対する補償に関する事項
- レ 再生医療等の提供に伴い、細胞提供者の健康、子孫に受け継がれ得る遺伝的特徴等に関する重要な知見が得られる可能性がある場合には、当該細胞提供者に係るその知見(偶発的所見を含む)の取扱い
- ソ 細胞提供者から取得された試料等について、当該細胞提供者から同意を得る時点では特定されない将来の研究のために用いられる可能性又は他の医療機関に提供する可能性がある場合には、その旨及び同意を受ける時点において想定される内容
- ツ 再生医療等の審査等業務(法第26条第1項に規定する審査等業務をいう)を行う認定再生医療等委員会(法第26条第5項第二号に規定する認定再生医療等委員会をいう)における審査事項その他当該再生医療等に係る認定再生医療等委員会に関する事項
- ネ 研究に用いる医薬品等(臨床研究法第2条第3項に規定する医薬品等をいう)の製造販売をし、若しくはしようとする医薬品等製造販売業者(同条第4項に規定する医薬品等製造販売業者をいう)又はその特殊関係者(同条第2項第一号に規定する特殊関係者をいう)による研究資金等(同号に規定する研究資金等をいう)の提供を受けて研究を行う場合においては、同法第32条に規定する契約の内容(研究として再生医療等を行う場合に限る)
- ナ その他当該細胞を用いる再生医療等の内容に応じ必要な事項
再生医療等を提供する医療機関の管理者は、再生医療等に特定細胞加工物を用いる場合、その特定細胞加工物の名称、構成細胞及び製造方法等を記載した特定細胞加工物概要書を作成しなければなりません(施行規則第8条第1項)。
再生医療等に特定細胞加工物を用いる場合において、再生医療等を提供する医療機関の管理者は、特定細胞加工物製造事業者に、法第44条に規定する特定細胞加工物製造事業者の業務に関し遵守すべき事項に従って細胞培養加工施設における特定細胞加工物の製造及び品質管理を行わせる必要があります(施行規則第8条第2項)。
施行規則第8条第2項によると、法第44条に規定する遵守事項に特定細胞加工物製造事業者を従わせることは、再生医療等提供機関の管理者の責務であることになります。
この規定中の「法第44条に規定する特定細胞加工物製造事業者の業務に関し遵守すべき事項」については「第四章 特定細胞加工物の製造」で具体的に説明します。
法第3条第2項第三号の基準(再生医療等技術の安全性の確保等に関する措置に関する事項)
上で説明した基準以外の、再生医療等技術の安全性の確保等に関する措置に関する基準には次のようなものがあります。
再生医療等を行う医師又は歯科医師の要件
再生医療等を行う医師又は歯科医師は、当該再生医療等を行うために必要な専門的知識及び十分な臨床経験を有していなければならず、研究として再生医療等を行う場合には、研究に関する倫理に配慮して当該研究を適正に実施するための十分な教育及び訓練を受けていなければなりません(施行規則第9条)。
再生医療等を行う際の責務と環境への配慮
医師又は歯科医師は、再生医療等を行う際には、次の責務を有します。
再生医療等を行う際の責務
| 条項 | いつ | 誰が | 何をする |
|---|---|---|---|
| 施行規則第10条 第1項 | 再生医療等を行う際 | 医師又は歯科医師 | 当該再生医療等の安全性及び妥当性について、科学的文献その他の関連する情報又は十分な実験の結果に基づき、倫理的及び科学的観点から十分検討する |
| 施行規則第10条 第2項 | 再生医療等に特定細胞加工物を用いる場合 | 医師又は歯科医師 | 特定細胞加工物製造事業者に特定細胞加工物の製造を行わせる際に、特定細胞加工物概要書に従った製造が行われるように必要な指示をする |
| 施行規則第10条 第3項 | 再生医療等に特定細胞加工物を用いる場合 | 医師又は歯科医師 | 再生医療等を受ける者に対して特定細胞加工物を投与する際に、当該特定細胞加工物が特定細胞加工物概要書に従って製造されたものか確認する等により、当該特定細胞加工物の投与の可否について決定する |
| 施行規則第10条 第4項 | 再生医療等を行う際 | 医師又は歯科医師 | 再生医療等安全性確保法施行規則、再生医療等提供計画及び研究計画書(研究として再生医療等を行う場合)に基づいて再生医療等を行う |
医師又は歯科医師は、環境に影響を及ぼすおそれのある再生医療等を行う場合には、環境へ悪影響を及ぼさないよう必要な配慮をする必要があります(施行規則第11条)。
再生医療等を受ける者の選定・その者に対する説明及び同意・個人情報の取扱い
医師又は歯科医師は、研究として再生医療等を行う際には、病状、年齢その他の事情を考慮した上で、再生医療等を受けることとなる者の選定をしなければなりません(施行規則第12条)。
再生医療等を行う医師又は歯科医師は、再生医療等を受ける者に対し、当該再生医療等について、文書により同意を得る必要があります(施行規則第13条第1項)。再生医療等を行う医師又は歯科医師は、この同意を得るに際し、次に掲げる事項について、できる限り平易な表現を用い、文書により再生医療等を受ける者に説明をします(施行規則第13条第2項)。
再生医療等を受ける者に説明する事項(施行規則第13条第2項)
- 提供する再生医療等の名称及び厚生労働大臣に再生医療等提供計画を提出している旨
- 再生医療等を提供する医療機関の名称並びに当該医療機関の管理者、実施責任者及び再生医療等を行う医師又は歯科医師の氏名(再生医療等を多施設共同研究として行う場合にあっては、代表管理者の氏名及び当該再生医療等を行う他の医療機関の名称及び当該医療機関の管理者の氏名を含む)
- 提供される再生医療等の目的及び内容
- 当該再生医療等に用いる細胞に関する情報
- 再生医療等を受ける者として選定された理由(研究として再生医療等を行う場合に限る)
- 当該再生医療等の提供により予期される利益及び不利益
- 再生医療等を受けることを拒否することは任意であること
- 同意の撤回に関する事項
- 再生医療等を受けることを拒否すること又は同意を撤回することにより不利益な取扱いを受けないこと。
- 研究に関する情報公開の方法(研究として再生医療等を行う場合に限る)
- 再生医療等を受ける者又は代諾者の求めに応じて、研究計画書その他の研究の実施に関する資料を入手又は閲覧できる旨及びその入手又は閲覧の方法(研究として再生医療等を行う場合に限る)
- 再生医療等を受ける者の個人情報の保護に関する事項
- 試料等の保管及び廃棄の方法
- 研究に対する施行規則第8条の8第1項各号に規定する関与に関する状況(研究として再生医療等を行う場合に限る)
- 苦情及び問合せへの対応に関する体制
- 当該再生医療等の提供に係る費用に関する事項
- 他の治療法の有無及び内容並びに他の治療法により予期される利益及び不利益との比較
- 当該再生医療等の提供による健康被害に対する補償に関する事項(研究として再生医療等を行う場合に限る)
- 再生医療等を受ける者の健康、子孫に受け継がれ得る遺伝的特徴等に関する重要な知見が得られる可能性がある場合には、当該者に係るその知見(偶発的所見を含む)の取扱い
- 再生医療等を受ける者から取得された試料等について、当該者から同意を受ける時点では特定されない将来の研究のために用いられる可能性又は他の医療機関に提供する可能性がある場合には、その旨と同意を受ける時点において想定される内容
- 当該再生医療等の審査等業務を行う認定再生医療等委員会における審査事項その他当該再生医療等に係る認定再生医療等委員会に関する事項
- 研究に用いる医薬品等の製造販売をし、若しくはしようとする医薬品等製造販売業者又はその特殊関係者による研究資金等の提供を受けて研究を行う場合においては臨床研究法第32条に規定する契約の内容(研究として再生医療等を行う場合に限る)
- その他当該再生医療等の提供に関し必要な事項
再生医療等を受ける者の代諾者に対する説明及び同意については施行規則第13条の規定を準用します。再生医療等を受ける者の代諾者の同意を得た場合には、再生医療等を行う医師又は歯科医師は、代諾者の同意に関する記録及び代諾者と再生医療等を受ける者との関係についての記録を作成します(施行規則第14条)。
細胞提供者及び再生医療等を受ける者に関する個人情報を保有する者は、特定の個人を識別することができないように保有する個人情報(「保有個人情報」)を加工する場合にあっては、必要な場合に特定の個人を識別できる情報を保有しつつ行った上で、当該個人情報を取り扱います(施行規則第23条)。
法第3条第2項第四号の基準(健康被害の補償の方法に関する事項)
法第3条第2項第四号において、厚生労働大臣は、再生医療等に用いる細胞を提供する者及び再生医療等(研究として行われる場合その他の厚生労働省令で定める場合に係るものに限る)を受ける者に対する健康被害の補償の方法に関する事項を定めるとされています。この「その他の厚生労働省令で定める場合」は、施行規則第21条において、「研究として行われる場合」とされています。これにより、再生医療等を受ける者に対しては、その再生医療等の提供が研究として行われる場合にのみ、健康被害の補償が行われるということになります。
再生医療等の提供を行う医療機関の管理者又は再生医療等に用いる細胞の提供を受ける医療機関等の管理者は、細胞提供者が再生医療等を受ける者以外の者である場合には、当該細胞の提供に伴い生じた健康被害の補償のために、保険への加入その他の必要な措置を講じておく必要があります(施行規則第22条第1項)。
再生医療等の提供を行う医療機関の管理者は、再生医療等(研究として行われる場合に限る)の提供に当たっては、当該再生医療等の提供に伴い生じた健康被害の補償のために、保険への加入その他の必要な措置を講じておく必要があります(施行規則第22条第2項)。
法第3条第2項第五号の基準(その他再生医療等の提供に関し必要な事項)
教育又は研修
再生医療等の提供を行う医療機関の管理者又は実施責任者は、再生医療等を適正に行うために定期的に教育又は研修の機会を確保する必要があります(施行規則第25条第1項)。それに対し、再生医療等を行う医師又は歯科医師その他の再生医療等に従事する者は、再生医療等を適正に行うために定期的に適切な教育又は研修を受け、情報収集に努めなければなりません(施行規則第25条第2項)。
苦情及び問い合わせへの対応
再生医療等の提供を行う医療機関の管理者は、苦情及び問合せに適切かつ迅速に対応するため、苦情及び問合せを受け付けるための窓口の設置、苦情及び問合せの対応の手順の策定その他の必要な体制の整備をする必要があります(施行規則第26条)。
認定再生医療等委員会の意見への対応
再生医療等の提供を行う医療機関の管理者は、認定再生医療等委員会から意見を述べられた場合には、当該意見を尊重して必要な措置を講じます(施行規則第26条の2)。
研究として再生医療等を実施する場合の再生医療等提供基準
以下において、研究として再生医療等を実施する場合に上記の基準に付け加えられる再生医療等の提供基準を紹介します。すぐに「第二節 再生医療等の提供の開始、変更及び中止の手続」の内容に移りたい方はこちらをクリック/タップしてください。
研究として再生医療等を実施する場合の再生医療等提供基準は、トグルをクリック/タップして開くことで現れます。
研究として再生医療等を行う場合の基本理念(施行規則第8条の2)
再生医療等が研究として行われるときは、再生医療等を受ける者の生命、健康及び人権を尊重し、次に掲げる事項を基本理念として行われる必要があります(施行規則第8条の2)。
再生医療等を研究として行うときの基本理念(施行規則第8条の2)
- 社会的及び学術的意義を有する研究を行うこと。
- 研究の分野の特性に応じた科学的合理性を確保すること。
- 研究により得られる利益及び再生医療等を受ける者への負担その他の不利益を比較考量すること。
- 独立した公正な立場における審査等業務を行う認定再生医療等委員会の審査を受けていること。
- 再生医療等を受ける者への事前の十分な説明を行うとともに、自由な意思に基づく同意を得ること。
- 社会的に特別な配慮を必要とする者について、必要かつ適切な措置を講ずること。
- 研究に利用する個人情報を適正に管理すること。
- 研究の質及び透明性を確保すること。
多施設共同研究(施行規則8条の3)
再生医療等を多施設共同研究として行う場合、その再生医療等に係る業務を代表するため、当該複数の施設の管理者の中から代表管理者を選任する必要があります(施行規則第8条の3第1項)。さらに、再生医療等を多施設共同研究として行う各医療機関の管理者は、当該再生医療等を行う他の医療機関の管理者と当該多施設共同研究に関連する必要な情報を共有しなければなりません(施行規則第8条の3第2項)。
研究計画書(施行規則第8条の4)
研究として再生医療等を行う医療機関の管理者は、次に掲げる事項を記載した研究計画書を作成します(施行規則第8条の4)。
研究計画書の内容(施行規則第8条の4)
- 研究の実施体制に関する事項
- 研究の背景に関する事項(当該研究に用いる細胞の概要に関する事項、特定細胞加工物の概要に関する事項及び再生医療等製品を用いる場合にあっては当該再生医療等製品の概要に関する事項を含む)
- 研究の目的に関する事項
- 研究の内容に関する事項(再生医療等提供計画に記載された再生医療等の内容をできる限り平易な表現を用いて記載したものを含む)
- 再生医療等を受ける者の選択及び除外並びに研究の中止に関する基準
- 再生医療等を受ける者に対する治療に関する事項
- 有効性の評価に関する事項
- 安全性の評価に関する事項
- 統計的な解析に関する事項
- 原資料等(研究により得られたデータその他の記録であって、臨床研究法第32条の規定により締結した契約の内容を含む)の閲覧に関する事項
- 品質管理及び品質保証に関する事項
- 倫理的な配慮に関する事項
- 記録(データを含む)の取扱い及び保存に関する事項
- 研究の実施に係る金銭の支払及び補償に関する事項
- 研究に関する情報の公表に関する事項
- 研究の実施期間
- 再生医療等を受ける者及び細胞提供者並びにこれらの代諾者に対する説明及びその同意(これらに用いる様式を含む)に関する事項
- 前各号に掲げるもののほか、研究の適正な実施のために必要な事項
モニタリング(施行規則第8条の5)
研究として再生医療等を行う医療機関の管理者は、研究計画書ごとにモニタリングに関する一の手順書を作成し、当該手順書及び研究計画書に定めるところにより、モニタリングを実施させる必要があります(施行規則第8条の5第1項)。しかしながら、モニタリングの対象となる研究に従事する者に、その者が直接担当する業務のモニタリングを行わせることはできません(施行規則第8条の5第2項)。
モニタリングに従事する者は、そのモニタリングの結果を、研究として再生医療等を行う医療機関の管理者に報告し、その管理者は、その報告を受け、再生医療等を多施設共同研究として行っている場合にあっては、必要に応じ、当該報告の内容を代表管理者に通知します(施行規則第8条の5第3項及び第4項)。
監査(施行規則第8条の6)
研究として再生医療等を行う医療機関の管理者は、必要に応じて、研究計画書ごとに監査に関する一の手順書を作成し、当該手順書及び研究計画書に定めるところにより、監査を実施させる必要があります(施行規則第8条の6第1項)。しかしながら、監査の対象となる研究に従事する者及びそのモニタリングに従事する者に、監査を行わせることはできません(施行規則第8条の6第2項)。
監査に従事する者は、その監査の結果を、研究として再生医療等を行う医療機関の管理者に報告し、その管理者は、その報告を受け、再生医療等を多施設共同研究として行っている場合にあっては、必要に応じ、当該報告の内容を代表管理者に通知します(施行規則第8条の6第3項及び第4項)。
モニタリング及び監査に従事する者の指導等(施行規則8条の7)
研究として再生医療等を行う医療機関の管理者は、モニタリングに従事する者及び監査に従事する者が行うモニタリング及び監査に関し、必要な指導及び管理を行う必要があります(施行規則第8条の7)。
利益相反管理計画の作成等(施行規則第8条の8)
研究として再生医療等を行う医療機関の管理者は、次に掲げる関与についての適切な取扱いの基準(「利益相反管理基準」)を定める必要があります(施行規則第8条の8第1項)。
利益相反管理基準の対象となる関与(施行規則第8条の8第1項)
- 研究として行う再生医療等に対する特定細胞加工物製造事業者又は医薬品等製造販売業者若しくはその特殊関係者による研究資金等の提供その他の関与
- 研究として行う再生医療等に従事する者(実施責任者、再生医療等を行う医師又は歯科医師及び統計的な解析を行うことに責任を有する者に限る。)及び研究計画書に記載されている者であって、当該研究を行うことによって利益を得ることが明白な者に対する当該研究に用いる特定細胞加工物の製造委託を受けている特定細胞加工物製造事業者又は当該研究に用いる医薬品等の製造販売をし、若しくはしようとする医薬品等製造販売業者若しくはその特殊関係者による寄附金、原稿執筆及び講演その他の業務に対する報酬の提供その他の関与
研究として再生医療等を行う医療機関の管理者又は所属機関の長は、施行規則第8条の8第1項に掲げる関与が確認された場合には、利益相反管理基準の確認及び利益相反管理基準に基づく事実関係についての確認を行い、その確認の結果(助言、勧告その他の措置が必要な場合にあっては、当該措置の内容を含む)を記載した報告書を作成します。研究として再生医療等を行う医療機関の管理者以外の者が当該報告書を作成したときは、当該医療機関の管理者に当該報告書を提出しなければなりません(施行規則第8条の8第2項)。
研究として再生医療等を行う医療機関の管理者は、前記報告書の内容も踏まえ、施行規則第8条の8第1項に掲げる関与についての適切な取扱いの方法を具体的に定めた計画(「利益相反管理計画」といい、前記報告書に助言、勧告その他の措置が記載されている場合にあっては、その内容を含む)を作成し、利益相反管理基準及び利益相反管理計画について、認定再生医療等委員会の意見を聴取します(施行規則第8条の8第3項及び第4項)。
研究として再生医療等を行う医療機関の管理者は、施行規則第8条の8第1項に掲げる関与について、利益相反管理基準及び利益相反管理計画に基づき、適切な管理を行わなければなりません(施行規則第8条の8第5項)。
施行規則第8条の8第1項及び第4項の規定は、再生医療等を多施設共同研究として行う場合について準用します。この場合において、第1項及び第4項中「研究として再生医療等を行う医療機関の管理者」とあるのは、「代表管理者」と読み替えます(施行規則第8条の8第6項)。
情報の公開(施行規則第8条の9)
研究として再生医療等を行う医療機関の管理者は、あらかじめ、研究を行うに当たり世界保健機関が公表を求める事項その他の研究の過程の透明性の確保及び国民の研究への参加の選択に資する事項を厚生労働省が整備するデータベースに記録することにより、これらの事項を公表し、これらを変更したときも同様に公表します(施行規則第8条の9第1項)。
研究として再生医療等を行う医療機関の管理者は、施行規則第8条の4第四号に掲げる研究の内容に関する事項として記載した主たる評価項目に係るデータの収集を行うための期間が終了したときは原則としてその日から一年以内に主要評価項目報告書を作成し、同号に掲げる研究の内容に関する事項として記載した全ての評価項目に係るデータの収集を行うための期間が終了したときは原則としてその日から一年以内に研究計画書につき一の総括報告書及びその概要を作成します(施行規則第8条の9第2項)。
研究として再生医療等を行う医療機関の管理者は、主要評価項目報告書の作成を行う場合は、法第5条第1項の再生医療等提供計画を変更する必要があります(施行規則第8条の9第3項)。
研究として再生医療等を行う医療機関の管理者は、主要評価項目報告書又は総括報告書及びその概要を作成したときは、認定再生医療等委員会の意見を聴いた上で、主要評価項目報告書又は総括報告書の概要について当該認定再生医療等委員会が意見を述べた日から起算して1月以内に各報告書を公表する必要があります(施行規則第8条の9第4項)。
研究として再生医療等を行う医療機関の管理者は、総括報告書の概要を公表しようとするときは、あらかじめ、これを厚生労働大臣に提出します(施行規則第8条の9第5項)。
研究として再生医療等を行う医療機関の管理者は、法第4条第1項若しくは第5条第1項の規定による再生医療等提供計画を提出をした場合、法第5条第3項の規定による再生医療等提供計画の軽微変更の届出をした場合又は施行規則第8条の9第5項の規定による統括報告書の概要の提出をした場合にあっては、公表を行ったものとみなします(施行規則第8条の9第6項)。
施行規則第8条の9第1項及び第3項から第6項までの規定は、再生医療等を多施設共同研究として行う場合について準用します(施行規則第8条の9第7項)。
個人情報の取扱い(施行規則第26条の3)
研究として再生医療等を行う医療機関の管理者及び研究として行う再生医療等に従事する者は、個人情報を取り扱うに当たっては、個人情報の保護に関する法律の規定によるほか、同法における個人に関する情報の保護の措置に準じて、個人情報の漏えい、滅失又は毀損の防止その他の個人情報の適切な管理のために必要な措置を講じる必要があります(施行規則第26条の3第1項)。
研究として再生医療等を行う医療機関の管理者及び研究として行う再生医療等に従事する者は、個人情報を取り扱うに当たっては、施行規則第26条の3第3項及び第4項並びに施行規則第26条の4から施行規則第26条の13までの規定に従います(施行規則第26条の3第2項)。
研究として行う再生医療等に従事する者は、原則として、あらかじめ、本人(個人情報によって識別される特定の個人をいいます)又はその親権を行う者、配偶者、後見人その他これらに準ずる者(以下「本人等」といいます)から同意を得た範囲又は施行規則第26条の4の規定により通知し、若しくは公表している範囲を超えて、再生医療等の実施に伴い取得した保有個人情報を取り扱うことはできません(施行規則第26条の3第3項)。
研究として再生医療等を行う医療機関の管理者は、個人情報の利用(再生医療等を多施設共同研究として行っている場合における他の医療機関の管理者又は外国にある者への提供を含む)の目的(「利用目的」)の達成に必要な範囲内において、保有個人情報を正確かつ最新の内容に保つ必要があります(施行規則第26条の3第4項)。
個人情報の利用に係る本人等の同意(施行規則第26条の4)
医師又は歯科医師は、個人情報を利用して研究として再生医療等を行う場合においては、次に掲げる場合を除き、本人等の同意を得る必要があります(施行規則第26条の4)。
本人等の同意を必要としない場合(施行規則第26条の4)
- 既存試料等(研究計画書が作成されるまでの間に存在する試料等又は当該研究計画書が作成された後に当該研究の目的以外の目的で取得された試料等であって、当該研究に利用するもの(特定細胞加工物に該当するものを除く)をいいます)の取得時に別の研究における利用についての同意が得られており、当該研究を行うことについて、次に掲げる事項を既存試料等が再生医療等に利用される者又はその親権を行う者、配偶者、後見人その他これらに準ずる者(「既存試料等が再生医療等に利用される者等」といいます)に通知し、又は公表しており、かつ、その同意が当該研究の目的と相当の関連性があると合理的に認められる場合
- イ 当該研究における既存試料等の利用目的及び利用方法(当該再生医療等を多施設共同研究として行う場合において、当該再生医療等を行う他の医療機関の管理者へ提供される場合はその方法を含む)
- ロ 当該研究に利用する既存試料等の項目
- ハ 当該研究に利用する既存試料等を利用する者の範囲
- ニ 当該研究に利用する既存試料等の管理について責任を有する者の氏名又は名称
- 当該研究の実施について、次に掲げる事項を既存試料等が再生医療等に利用される者等に通知し、又は公表している場合であって、当該既存試料等が再生医療等に利用される者が当該研究に参加することについて、原則として、既存試料等が再生医療等に利用される者等が拒否できる機会を保障している場合(前号に該当する場合を除く)
- イ 前号イからニまでに掲げる事項
- ロ 既存試料等が再生医療等に利用される者等の求めに応じて、既存試料等が再生医療等に利用される者が識別される既存試料等の利用(当該再生医療等を多施設共同研究として行う場合における当該再生医療等を行う他の医療機関の管理者への提供を含む)を停止すること
- ハ ロの既存試料等が再生医療等に利用される者等の求めを受け付ける方法
試料等に係る個人情報の保護に関する措置(施行規則第26条の12)
再生医療等を多施設共同研究として行う各医療機関の管理者は、当該再生医療等を行う他の医療機関の管理者に対し試料等を提供する場合にあっては、特定の個人を識別することができないように加工するよう努力します(施行規則第26条の12)。
記録の作成(施行規則第26条の13)
外国にある者と共同して研究を行う場合であって、外国にある者に保有個人情報を含む試料等を提供するとき(他の法令の規定により当該外国にある者に当該試料等を提供する場合を除く)には、研究として再生医療等を行う医療機関の管理者は、次に掲げる事項に関する記録を作成する必要があります(施行規則第26条の13第1項)。
外国にある者に保有個人情報を含む試料等を提供するときの記録事項(施行規則第26条の13第1項)
- 当該保有個人情報を含む試料等を提供した年月日
- 当該外国にある者の名称及び所在地
- 法第14条に規定する同意を得ている旨又は前条に規定する手続を行っている旨
- 当該保有個人情報によって識別される本人の氏名その他の当該本人を特定するに足りる事項
- 当該外国にある者に提供した保有個人情報の項目
外国にある者から個人情報を含む試料等の提供を受ける場合(他の法令の規定により外国にある者から試料等の提供を受ける場合を除く)には、研究として再生医療等を行う医療機関の管理者は、次に掲げる事項の確認を行い、当該確認に係る事項に関する記録を作成する必要があります(施行規則第26条の13第2項)。
外国にある者から個人情報を含む試料等の提供を受ける場合の確認事項(施行規則第26条の13第2項)
- 当該個人情報を含む試料等の提供を受けた年月日
- 当該試料等の提供を行った外国にある者の名称及び所在地
- 当該試料等が適切に取得されたことを記載した書類
- 当該外国にある者から提供を受けた個人情報の項目
第一節のまとめ
ここまで、再生医療等提供基準に係る規定を紹介しました。再生医療等を提供しようとする医療機関は、上記の基準を満たすよう、その医療機関の規則・細則の中にこれらの基準に対応する規定を設けて体制を整備します。
第二節 再生医療等の提供の開始、変更及び中止の手続
第一款 通則
再生医療等を提供しようとする病院又は診療所の管理者は、あらかじめ、第一種再生医療等、第二種再生医療等及び第三種再生医療等のそれぞれの区分ごとに、再生医療等の提供に関する計画(「再生医療等提供計画」)を厚生労働大臣に提出しなければなりません(法第4条第1項)。
ただし、厚生労働大臣に再生医療等提供計画を提出する前に、その再生医療等提供計画が再生医療等提供基準に適合しているかどうかについて認定再生医療等委員会の意見を聴く必要があります(法第4条第2項)。
再生医療等提供計画には次の事項の記載が必要です。
再生医療等提供計画の記載事項(法第4条第1項)
- 当該病院又は診療所の名称及び住所並びに当該管理者の氏名
- 提供しようとする再生医療等及びその内容
- 前号に掲げる再生医療等について当該病院又は診療所の有する人員及び構造設備その他の施設
- 第二号に掲げる再生医療等に用いる細胞の入手の方法並びに当該再生医療等に用いる特定細胞加工物の製造及び品質管理の方法(特定細胞加工物の製造を委託する場合にあっては、委託先の名称及び委託の内容)
- 前二号に掲げるもののほか、第二号に掲げる再生医療等に用いる再生医療等技術の安全性の確保等に関する措置
- 第二号に掲げる再生医療等に用いる細胞を提供する者及び当該再生医療等(研究として行われる場合その他の厚生労働省令で定める場合に係るものに限る)を受ける者に対する健康被害の補償の方法
- 第二号に掲げる再生医療等について第26条第1項各号に掲げる業務を行う認定再生医療等委員会(同条第5項第二号に規定する認定再生医療等委員会をいう。以下この章において同じ)の名称及び委員の構成
- その他厚生労働省令で定める事項
法第4条第1項第六号の厚生労働省令で定める場合は、研究として行われる場合です(施行規則第27条第3項)。
法第4条第1項第八号の厚生労働省令で定める事項は、次に掲げる事項です(施行規則第27条第4項)。
法第4条第1項第八号の厚生労働省令で定める事項(施行規則第27条第4項)
- 審査等業務を行う認定再生医療等委員会の認定番号及び再生医療等提供計画の審査に関する事項
- 個人情報の取扱いの方法
- 教育又は研修の方法
- 苦情及び問合せへの対応に関する体制の整備状況
- 前各号に掲げるもののほか、再生医療等を提供するに当たって留意すべき事項
法第4条第1項の規定による提出を行う際、研究として再生医療等を行う場合とそれ以外の場合とでは再生医療等提供計画の提出に用いる書式が異なっています(施行規則第27条第1項)。研究として再生医療等を行う場合では様式第一の書式を使用し、それ以外の場合では様式第一の二の書式を使用します。
再生医療等提供計画の提出に際しては、認定再生医療等委員会がその審査においてまとめた意見を記載した書類及びその他厚生労働省令で定める書類と共に再生医療等提供計画を提出します(法第4条第3項)。
この「その他厚生労働省令で定める書類」は、次の書類になります(施行規則第27条第8項)。
再生医療等提供計画の提出に際して再生医療等提供計画と共に提出される厚生労働省令で定める書類(施行規則第27条第8項)
- 提供する再生医療等の詳細を記した書類(研究として再生医療等を行う場合は、研究計画書)
- 実施責任者及び再生医療等を行う医師又は歯科医師の氏名、所属、役職及び略歴(研究に関する実績がある場合には、当該実績を含む)を記載した書類
- 再生医療等提供計画に記載された再生医療等と同種又は類似の再生医療等に関する国内外の実施状況を記載した書類
- 特定細胞加工物を用いる場合にあっては、再生医療等提供計画に記載された再生医療等に用いる細胞に関連する研究を記載した書類
- 特定細胞加工物を用いる場合にあっては、特定細胞加工物概要書、施行規則第96条に規定する特定細胞加工物標準書、施行規則第97条第1項に規定する衛生管理基準書、同条第2項に規定する製造管理基準書及び同条第3項に規定する品質管理基準書
- 再生医療等製品を用いる場合にあっては、当該再生医療等製品の注意事項等情報(薬機法第68条の2第2項に規定する注意事項等情報)
- 特定細胞加工物の製造を委託する場合にあっては、委託契約書の写しその他これに準ずるもの
- 削除
- 施行規則第8条の5の規定により作成した手順書及び施行規則第8条の6の規定により手順書を作成した場合にあっては、当該手順書(研究として再生医療等を行う場合に限る)
- 利益相反管理基準及び利益相反管理計画(研究として再生医療等を行う場合に限る)
- 統計解析計画書(統計的な解析を行うための計画書)を作成した場合にあっては、当該統計解析計画書(研究として再生医療等を行う場合に限る)
再生医療等の提供の開始時の提出書類のまとめ
- 再生医療等提供計画
- 認定再生医療等委員会の意見書
- その他厚生労働省令で定める書類
再生医療等提供計画の変更
さらに、再生医療等提供計画を変更する場合にも、変更後の再生医療等を提供しようとする病院又は診療所の管理者は、あらかじめ、厚生労働大臣に対して手続きを行うことが必要になります(法第5条第1項)。この再生医療等提供計画の変更手続には法第4条第2項及び第3項の規定を準用します(法第5条第2項)。
法第5条第1項の規定によって再生医療等提供計画を変更するときは、変更後の再生医療等提供計画及び様式第二による届書を提出して行います。再生医療等を多施設共同研究として行う場合にあっては、その多施設共同研究の代表管理者がこの提出を行います(施行規則第28条)。
再生医療等提供計画の変更が軽微である場合では新たに再生医療等提供計画を提出する必要はなく、軽微変更から10日以内の認定再生医療等委員会への通知と厚生労働大臣への届出でよしとされています(法第5条第3項)。
この軽微な変更は厚生労働省令で定められており、次の事項が軽微変更から除外されています。
軽微変更から除外される事項(施行規則第29条)
- 当該再生医療等の安全性に影響を与える再生医療等の提供方法の変更
- 特定細胞加工物を用いる場合にあっては、当該再生医療等の安全性に影響を与える特定細胞加工物の製造及び品質管理の方法の変更
- 再生医療等製品を用いる場合にあっては、当該再生医療等製品に係る薬機法施行規則第137条の28第四号に掲げる変更
- 再生医療等が研究として行われる場合にあっては、研究の実施方法の変更
- 前各号に掲げる変更のほか、当該再生医療等の安全性に影響を与えるもの
法第5条第3項の規定による再生医療等提供計画の軽微変更の届出は、様式第三による届書を提出して行います。再生医療等を多施設共同研究として行う場合にあっては、その多施設共同研究の代表管理者がこの届出を行います(施行規則第30条)。
認定再生医療等委員会の変更禁止
提供機関管理者(再生医療等提供機関の管理者のこと)は、法第4条第1項の規定により、再生医療等提供計画を厚生労働大臣に提出した後は、認定再生医療等委員会が廃止された場合その他のやむを得ない事情がある場合を除き、再生医療等提供計画に記載されている認定再生医療等委員会を変更することができません(施行規則第30条の2)。
再生医療等の提供の中止及び提供の終了
再生医療等提供計画に記載された再生医療等の提供を中止する場合にも、再生医療等の提供を中止する病院又は診療所の管理者は、厚生労働大臣に対して手続きを行うことが必要になります。
再生医療等提供機関の管理者は、再生医療等提供計画に記載された再生医療等の提供を中止したときは、厚生労働省令で定めるところにより、その中止の日から10日以内に、その旨を、再生医療等提供計画に記載された認定再生医療等委員会に通知するとともに、厚生労働大臣に届け出なければなりません(法第6条)。
法第6条の規定により再生医療等提供計画に記載された再生医療等の提供を中止するときは、様式第四による届書を提出して行います。法第6条の規定による通知及び前項の規定による届出は、再生医療等を多施設共同研究として行っている場合にあっては、その多施設共同研究の代表管理者がこの届出及び法第6条の規定による認定再生医療等委員会への通知を行います(施行規則第31条)。
提供機関管理者は、再生医療等提供計画に記載された再生医療等(研究として行われる場合を除く)の提供を終了したときは、遅滞なく、その旨を、再生医療等提供計画に記載された認定再生医療等委員会に通知するとともに、厚生労働大臣に届け出なくてはなりません(施行規則第31条の2)。
再生医療等の提供の開始、変更及び中止・終了のまとめ
再生医療等の提供の開始、変更及び中止・終了に必要な手続
開始時の手順
1.再生医療等提供計画の作成
2.認定再生医療等委員会への諮問
3.厚生労働大臣への再生医療等提供計画の提出
変更時の手順
1.変更を含む再生医療等提供計画の作成
2.認定再生医療等委員会への諮問
3.厚生労働大臣への再生医療等提供計画の提出
中止時の手続(中止から10日以内)
・認定再生医療等委員会への通知
・厚生労働大臣への届出
終了時の手続(遅滞なく:概ね1週間~2週間以内)
・認定再生医療等委員会への通知
・厚生労働大臣への届出
厚生労働大臣による情報の公表
厚生労働大臣は、再生医療等提供機関が提供する再生医療等に係る次の各号に掲げる事項(法第5条第3項の規定による再生医療等提供計画の軽微変更の届出があった場合には、当該各号に掲げる事項であって当該届出に係る変更後のもの)をインターネットを利用して公衆の閲覧に供する方法により公表します(施行規則第31条の3)。
厚生労働大臣により公表される事項(施行規則第31条の3)
- 再生医療等提供機関の名称及び住所並びに管理者の氏名
- 提供する再生医療等(研究として行われる場合にあっては、その旨を含む)及び再生医療等の区分
- 再生医療等提供計画に記載された認定再生医療等委員会の名称
- 再生医療等を受ける者に対する説明文書及び同意文書の様式
- 法第22条又は第23条の規定による命令(提供機関管理者が法第4条第1項の規定による提出を行うことなく他の再生医療等を提供した場合に行うものを含む)をした場合にあっては、その内容
認定再生医療等委員会のうち、第一種再生医療等及び第二種再生医療等の提供計画がそれぞれの再生医療等提供基準に合致するか審査する能力を有する者から構成されている認定再生医療等委員会を特定認定再生医療等委員会といいます。したがって、特定認定再生医療等委員会ではないただの認定再生医療等委員会は、第三種再生医療等提供計画についてのみ意見を述べることができます。
ここからは、第一種再生医療等及び第二種再生医療等の提供に関する特則を紹介します。
第二款 第一種再生医療等の提供に関する特則
第一種再生医療等提供機関の管理者からその第一種再生医療等提供計画についての意見を聴取される認定再生医療等委員会は特定認定再生医療等委員会です(法第7条)。
第一種再生医療等提供計画の提出があった場合、厚生労働大臣は、当該提供計画に記載された第一種再生医療等が再生医療等提供基準に適合していないと認めるときは、その提出日から90日以内に限り、当該提供計画に係る再生医療等提供機関の管理者に対して提供計画の変更その他必要な措置をとるように命令することができます。厚生労働大臣は、必要に応じてこの90日の期間を延長又は短縮することができ、この期間を延長又は短縮した場合には再生医療等提供機関の管理者に対して延長後又は短縮後の期間を通知します(法第8条)。
また、当該提供計画に係る第一種再生医療等提供機関は、この期間内に当該第一種再生医療等を提供してはなりません(法第9条)。
法第8条及び法第9条の規定は、第一種再生医療等提供計画を変更し、新たに第一種再生医療等提供計画を提出した場合にも準用しますが、法第8条に規定する期間が経過していない間では変更前の第一種再生医療等提供計画に従って第一種再生医療等を提供することができます(法第10条)。
第一種再生医療等提供計画の提供を受けた厚生労働大臣は、当該第一種再生医療等提供計画の変更その他の命令を出す際には厚生科学審議会の意見を聴取することになっています(法第55条第4項)。
第三款 第二種再生医療等の提供に関する特則
第二種再生医療等提供機関の管理者からその第二種再生医療等提供計画についての意見を聴取される認定再生医療等委員会は特定認定再生医療等委員会です(法第11条)。
第二節のまとめ
第一種再生医療等、第二種再生医療等、及び第三種再生医療等の提供開始に係る手続の流れは、次図のようにまとまります。
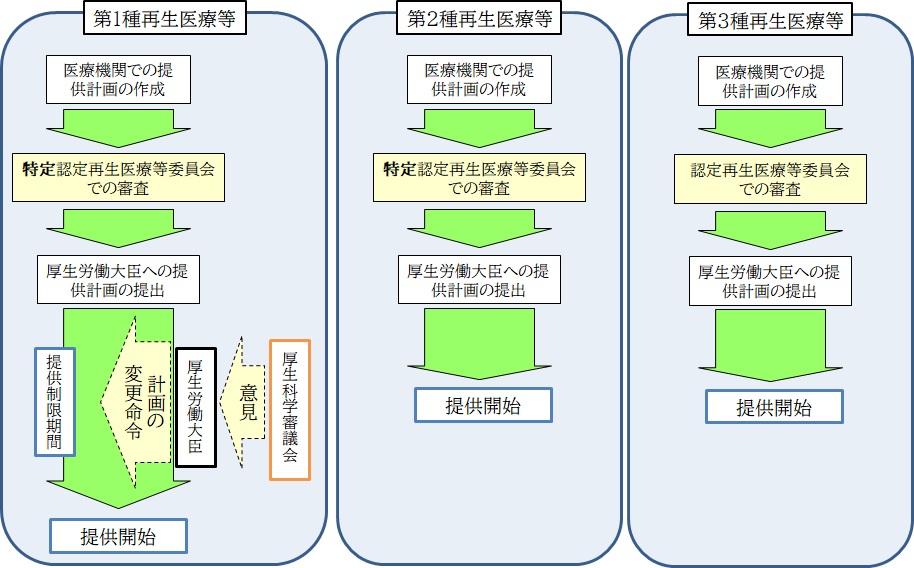
この図から判るように、厚生労働大臣への再生医療等提供計画の提出後、再生医療等を提供しようとする病院又は診療所は、第二種再生医療等及び第三種再生医療等についてはすぐに提供を開始することができます。
第三節 再生医療等の適正な提供に関する措置
再生医療等安全性確保法は、再生医療等が適正に提供されるよう、次の措置を講じています。
特定細胞加工物の製造の委託(法第12条)
再生医療等提供機関の管理者は、特定細胞加工物の製造を委託しようとするときは、必ず特定細胞加工物製造事業者に委託します。
再生医療等提供計画の確認(法第13条)
医師又は歯科医師は、再生医療等を行おうとするときは、次に掲げる事項を確認します。
- 当該再生医療等が提出済みの再生医療等提供計画に記載された再生医療等であること
- 当該再生医療等が第一種再生医療等である場合には当該第一種再生医療等に係る第一種再生医療等提供計画について法第9条(法第10条第1項において準用する場合を含む)に規定する期間が経過していること
再生医療等の説明及び同意(インフォームド・コンセント)の取得(法第14条)
再生医療等を行うに当たり、医師又は歯科医師は、疾病のため本人の同意を得ることが困難な場合その他の厚生労働省令で定める場合を除き、その再生医療等を受ける者に対し、当該再生医療等の適正な提供のために必要な事項(当該再生医療等に用いる再生医療等技術の安全性の確保等の事項)について適切な説明を行い、同意を得る必要があります(法第14条第1項)。
法第14条第1項の厚生労働省令で定める場合は、次に掲げる場合です(施行規則第32条)。
再生医療等に用いる当たり当該再生医療等の受給者の同意取得が免除される厚生労働省令で定める場合(施行規則第32条)
- 単独で説明を受け、同意を与えることが困難な者に対し、再生医療等を行う場合であって、次に掲げる場合のいずれかに該当する場合
- イ 当該再生医療等を行うことに合理的理由があることについて、認定再生医療等委員会の審査を受けた場合であって、次の(1)から(5)までのいずれも満たす場合
- (1) 当該再生医療等を受けることとなる者に緊急かつ明白な生命の危険が生じていること。
- (2) その他の治療方法では十分な効果が期待できないこと。
- (3) 当該再生医療等を受けることにより生命の危険が回避できる可能性が十分にあると認められること。
- (4) 当該再生医療等を受けることとなる者に対する予測される不利益が必要な最小限度のものであること。
- (5) 代諾者となるべき者と直ちに連絡を取ることができないこと。
- ロ イの場合以外の場合であって、当該再生医療等を行うことに合理的理由があることについて、認定再生医療等委員会の審査を受けており、当該再生医療等を受けることとなる者の代諾者の同意を得ている場合
- イ 当該再生医療等を行うことに合理的理由があることについて、認定再生医療等委員会の審査を受けた場合であって、次の(1)から(5)までのいずれも満たす場合
- 十六歳未満の者に対し、再生医療等を行う場合であって、次に掲げる場合のいずれかに該当する場合(前号に掲げる場合を除く。)
- イ 当該再生医療等を受けることとなる者が再生医療等を受けることについての説明を十分理解できる能力を有しており、当該者の理解を得ている場合であって、前号イの(1)から(5)までのいずれも満たす場合
- ロ イの場合以外の場合であって、当該再生医療等を受けることとなる者が再生医療等を受けることについての説明を十分理解できる能力を有し、かつ、当該者の理解を得ており、当該再生医療等を受けることとなる者の代諾者の同意を得ている場合
再生医療等を受ける者以外の者から再生医療等に用いる細胞の採取を行うに当たり、医師又は歯科医師は、疾病のため本人の同意を得ることが困難な場合その他の厚生労働省令で定める場合を除き、その細胞を提供する者(細胞提供者)に対し、採取した細胞の使途その他当該細胞の採取に関し必要な事項について適切な説明を行い、同意を得る必要があります(法第14条第2項)。
法第14条第2項の厚生労働省令で定める場合は、次に掲げる場合です(施行規則第33条)。
再生医療等に用いる細胞の採取に当たり細胞提供者の同意取得が免除される厚生労働省令で定める場合(施行規則第33条)
- 単独で説明を受け、同意を与えることが困難な者から再生医療等に用いる細胞の採取を行う場合であって、次に掲げる場合のいずれかに該当する場合
- イ 当該採取を行うことに合理的理由があることについて、認定再生医療等委員会の審査を受けた場合であって、次の(1)及び(2)を満たす場合
- (1) 当該細胞を採取されることとなる者が、あらかじめ、再生医療等に用いられるために自らの細胞を提供する意思を表示していること。
- (2) 代諾者となるべき者と直ちに連絡を取ることができないこと。
- ロ イの場合以外の場合であって、当該採取を行うことに合理的理由があることについて、認定再生医療等委員会の審査を受けており、当該細胞を採取されることとなる者の代諾者の同意を得ている場合
- イ 当該採取を行うことに合理的理由があることについて、認定再生医療等委員会の審査を受けた場合であって、次の(1)及び(2)を満たす場合
- 十六歳未満の者から再生医療等に用いる細胞の採取を行う場合であって、次に掲げる場合のいずれかに該当する場合(前号に掲げる場合を除く。)
- イ 当該細胞を採取されることとなる者が当該細胞の採取を行うことについての説明を十分理解できる能力を有しており、当該者の理解を得ている場合であって、前号イの(1)及び(2)を満たす場合
- ロ イの場合以外の場合であって、当該細胞を採取されることとなる者が当該細胞の採取を行うことについての説明を十分理解できる能力を有し、かつ、当該者の理解を得ており、当該細胞を採取されることとなる者の代諾者の同意を得ている場合
再生医療等に関する個人情報の保護(法第15条)
再生医療等提供機関の管理者は、再生医療等に用いる細胞の提供者及び再生医療等を受ける者の個人情報の漏えい、滅失又は毀損の防止その他の個人情報の適切な管理のために必要な措置を講じる必要があります。
再生医療等に関する記録及び保存(法第16条)
再生医療等を行ったときは、厚生労働省令で定めるところにより、医師又は歯科医師は、当該再生医療等の実施の日時及び場所、当該再生医療等の内容その他の厚生労働省令で定める事項に関する記録を作成しなければならず(法第16条第1項)、再生医療等提供機関の管理者は、その記録を厚生労働省令で定めるところによって保存しなければなりません(法第16条第2項)。
この記録は、再生医療等を受けた者ごとに作成されることになっており(施行規則第34条第1項)、法第16条中の「厚生労働省令で定める事項」には次の事項が挙げられます(施行規則第34条第2項)。
再生医療等に関する記録事項(施行規則第34条第2項)
- 再生医療等を行う場合 次に掲げる事項
- イ 再生医療等を受けた者の住所、氏名、性別及び生年月日
- ロ 病名及び主要症状
- ハ 使用した特定細胞加工物又は再生医療等製品の種類、投与方法その他の再生医療等の内容及び評価
- ニ 再生医療等に用いる細胞に関する情報
- ホ 特定細胞加工物の製造を委託した場合は委託先及び委託業務の内容
- ヘ 再生医療等を行った年月日
- ト 再生医療等を行った医師又は歯科医師の氏名
- チ イからトまでに掲げるもののほか、再生医療等を行うために必要な事項
- 研究として再生医療等を行う場合 次に掲げる事項
- イ 再生医療等を受ける者を特定する事項
- ロ 再生医療等を受ける者に対する診療及び検査に関する事項
- ハ 研究への参加に関する事項
- ニ イからハまでに掲げるもののほか、研究として再生医療等を行うために必要な事項
提供機関管理者は、再生医療等が行われたとき(研究として再生医療等を行ったときを除く)は、次に掲げる書類を、次に掲げる再生医療等の態様に応じ、次の各号に掲げる期間、保存します(施行規則第34条第3項)。
保存する書類(施行規則第34条第3項)
- 法第16条第1項の規定による施行規則第34条第2項第一号に関する再生医療等の記録
- 再生医療等提供計画
- 施行規則第27条第8項第一号から第八号までに掲げる書類
- 再生医療等を受ける者及び細胞提供者並びにこれらの代諾者に対する説明及びその同意に係る文書
- 認定再生医療等委員会から受け取った審査等業務に係る文書
再生医療等の態様と保存期間(施行規則第34条第3項)
| 施行規則 | 再生医療等の態様 | 保存期間 |
|---|---|---|
| 第34条 第3項第一号 | 指定再生医療等製品(薬機法第68条の7第3項に規定する指定再生医療等製品であって、同法第23条の25又は第23条の37の承認の内容に従わずに用いるものに限る)又は指定再生医療等製品の原料と類似の原料から成る特定細胞加工物を用いた場合 | 30年間 |
| 第34条 第3項第二号 | 前号に掲げる指定再生医療等製品又は特定細胞加工物以外の細胞加工物を用いた場合 | 10年間 |
提供機関管理者は、研究として再生医療等が行われたときは、法第16条の第1項の規定による施行規則第34条第2項第二号に関する再生医療等の記録を、次に掲げる書類と共に、研究終了日から5年間保存します(施行規則第34条第4項)。
再生医療等の記録と共に保存する書類(施行規則第34条第4項)
- 総括報告書その他のこの省令の規定により再生医療等を提供する医療機関の管理者、実施責任者又は再生医療等を行う医師若しくは歯科医師が作成した文書又はその写し及び記録
- モニタリング及び監査(施行規則第8条の6の規定により監査を実施する場合に限る)に関する文書
- 原資料等(法第16条、施行規則第34条第3項及び第一号に掲げるものを除く)
- 研究の実施に係る契約書(臨床研究法第32条の規定により締結した契約に係るものを除く)
- 前各号のほか、再生医療等を研究として行うために必要な文書
各機関への疾病等の報告(法第17条~第21条)
トラブル発生時の報告
(認定再生医療等委員会へのトラブル報告)
再生医療等提供機関の管理者は、再生医療等提供計画に記載された再生医療等の提供に起因するものと疑われる疾病、障害若しくは死亡又は感染症の発生を知ったときは、厚生労働省令で定めるところにより、その旨を認定再生医療等委員会に報告しなければならず、認定再生医療等委員会が当該報告に対して意見を述べたときは、その意見を尊重して必要な措置をとらなければなりません(法第17条)。
このときの認定再生医療等委員会へのトラブル報告について、提供機関管理者は、次の各号に掲げる事項を知ったときは、それぞれ当該各号に定める期間内に当該事項を認定再生医療等委員会に報告します(施行規則第35条第1項)。
第一号(7日)
次に掲げる疾病等の発生のうち、当該再生医療等の提供によるものと疑われるもの又は当該再生医療等の提供によるものと疑われる感染症によるもの
(イ)死亡
(ロ)死亡につながるおそれのある症例
第二号(15日)
次に掲げる疾病等の発生のうち、当該再生医療等の提供によるものと疑われるもの又は当該再生医療等の提供によるものと疑われる感染症によるもの
(イ)治療のために医療機関への入院又は入院期間の延長が必要とされる症例
(ロ)障害
(ハ)障害につながるおそれのある症例
(ニ)重篤である症例
(ホ)後世代における先天性の疾病又は異常
第三号(再生医療等提供計画を厚生労働大臣に提出した日から起算して60日ごとに当該期間満了後10日以内)
再生医療等の提供によるものと疑われる又は当該再生医療等の提供によるものと疑われる感染症による疾病等の発生(前二号に掲げるものを除く)
施行規則第35条第1項の規定は、再生医療等を多施設共同研究として行う場合について準用します(施行規則第35条第2項)。この場合、「代表管理者」が認定再生医療等委員会への報告を行います。
(厚生労働大臣へのトラブル報告)
また、再生医療等提供機関の管理者は、再生医療等提供計画に記載された再生医療等の提供に起因するものと疑われる疾病、障害若しくは死亡又は感染症の発生に関する事項で厚生労働省令で定めるものを知ったときは、厚生労働省令で定めるところにより、その旨を厚生労働大臣に報告しなければなりません(法第18条)。
法第18条の厚生労働省令で定める事項は、施行規則第35条第1項第一号及び第二号に掲げる事項です(施行規則第36条第1項)。さらに、施行規則第35条(第1項第三号を除く)の規定は、この法第18条の規定による厚生労働大臣への報告に準用します(施行規則第36条第2項)。この場合、提供機関管理者は、「厚生労働大臣」に対して報告を行います。
厚生労働大臣は、法第18条の規定による報告の状況について厚生科学審議会に報告し、必要があると認めるときは、厚生科学審議会の意見を聴いて、再生医療等の提供による保健衛生上の危害の発生又は拡大を防止するために必要な措置をとります(法第19条第1項)。厚生科学審議会は、前項の規定による措置のほか、再生医療等の提供による保健衛生上の危害の発生又は拡大を防止するために必要な措置について、調査審議し、必要があると認めるときは、厚生労働大臣に意見を述べることができます(同条第2項)。
定期報告
(認定再生医療等委員会への定期報告)
再生医療等提供機関の管理者は、再生医療等提供計画に記載された再生医療等の提供の状況について、厚生労働省令で定めるところにより、定期的に認定再生医療等委員会に報告しなければならず、認定再生医療等委員会が当該報告に対して意見を述べたときは、その意見を尊重して必要な措置をとらなければなりません(法第20条)。
法第20条の規定に基づき、提供機関管理者は、再生医療等提供計画に記載された再生医療等技術ごとに、当該再生医療等提供計画に記載された認定再生医療等委員会に、次に掲げる事項を報告します(施行規則第37条第1項)。
再生医療等の提供の状況についての認定再生医療等委員会への定期報告の内容(施行規則第37条第1項)
- 当該再生医療等を受けた者の数
- 当該再生医療等に係る疾病等の発生状況及びその後の経過
- 当該再生医療等の安全性及び科学的妥当性についての評価
- 当該再生医療等に対する施行規則第8条の8第1項各号に規定する関与に関する事項
- 当該再生医療等に係るこの省令又は再生医療等提供計画に対する不適合の発生状況及びその後の対応
この報告には施行規則第27条第8項各号に掲げる書類(認定再生医療等委員会が有しない最新のものに限る)を添付します(施行規則第37条第2項)。さらに、この報告は、再生医療等提供計画を厚生労働大臣に提出した日から起算して、一年ごとに、当該期間満了後90日以内に行われる必要があります(施行規則第37条第3項)。
報告を受けた認定再生医療等委員会は、当該再生医療等の継続の適否について意見を述べます(施行規則第37条第4項)。
施行規則第37条第1項~第4項の規定は、再生医療等を多施設共同研究として行う場合について準用します(施行規則第37条第5項)。
(厚生労働大臣への定期報告)
また、再生医療等提供機関の管理者は、再生医療等提供計画に記載された再生医療等の提供の状況について、厚生労働省令で定めるところにより、定期的に厚生労働大臣に報告しなければならず、厚生労働大臣は、当該報告を取りまとめ、その概要を公表しなければなりません(法第21条)。
法第21条第1項の規定に基づき、提供機関管理者は、再生医療等提供計画に記載された再生医療等技術ごとに、厚生労働大臣に、次に掲げる事項を報告します(施行規則第38条第1項)。
再生医療等の提供の状況についての厚生労働大臣への定期報告の内容(施行規則第38条第1項)
- 当該再生医療等提供計画に記載されている認定再生医療等委員会の名称
- 当該認定再生医療等委員会による当該再生医療等の継続の適否に係る意見
- 施行規則第37条第1項第一号に掲げる事項(当該再生医療等を受けた者の数)
この報告には施行規則第27条第8項各号に掲げる書類(厚生労働大臣が有しない最新のものに限る)を添付します(施行規則第38条第2項)。施行規則第37条第1項の報告に対し認定再生医療等委員会が意見を述べた場合には、提供機関管理者は、第1項に規定する厚生労働大臣への報告の際には、認定再生医療等委員会の意見を添える必要があります(施行規則第38条第3項)。さらに、この報告は、再生医療等提供計画を厚生労働大臣に提出した日から起算して、一年ごとに、当該期間満了後90日以内に行われる必要があります(施行規則第38条第4項)。
施行規則第38条第1項~第4項の規定は、再生医療等を多施設共同研究として行う場合について準用します(施行規則第38条第5項)。
命令と立入検査等(第22条~第24条)
厚生労働大臣は、必要があると認めるときは、次の命令をすることができます。
厚生労働大臣の命令
| 緊急命令 (法第22条) | 改善命令等 (法第23条第1項) | 改善命令等 (法第23条第2項) | |
|---|---|---|---|
| 目的 | 再生医療等の提供による保健衛生上の危害の発生又は拡大の防止 | 再生医療等技術の安全性の確保等その他再生医療等の適正な提供 | 第1項に同じ |
| 被命令者 | 再生医療等を提供する病院又は診療所の管理者 | 再生医療等提供機関の管理者 | 第1項に同じ |
| 命令発令のタイミング | 必要があると認めたとき | 必要があると認めたとき | 第1項による命令に従わないとき |
| 命令の内容 | ・当該再生医療等の提供の一時停止 ・その他の保健衛生上の危害の発生又は拡大を防止するための応急の措置 | ・再生医療等提供計画の変更 ・その他の再生医療等の適正な提供に関する必要な措置 | ・再生医療等提供計画に記載された再生医療等の全部又は一部の提供の一定期間の制限 |
厚生労働大臣は、必要に応じて再生医療等提供機関の管理者若しくは開設者(法第24条第1項)又は病院若しくは診療所の管理者(法第24条第2項)に対し、必要な報告をさせ、又は当該職員に、当該機関(病院若しくは診療所)に立ち入り、その構造設備若しくは帳簿、書類その他の物件を検査させ、若しくは関係者に質問させることができます。
調査の範囲/タイミング
| 法第24条第1項 | 法第24条第2項 |
|---|---|
| 再生医療等の提供に係る規定の施行に必要な範囲 | 再生医療等の提供に係る規定若しくはその規定に基づく命令若しくは処分に違反していると認めるとき、又は再生医療等技術の安全性の確保等その他再生医療等の適正な提供のため必要があると認めるとき |
再生医療等の提供に係る規定とは、法第3条~第25条の規定をいいます。
厚生労働大臣は、法第24条第1項の規定により提供機関管理者若しくは開設者(医療法第5条第1項に規定する医師又は歯科医師を含む)に対して必要な報告をさせるとき又は法第24条第2項の規定により医療機関の管理者若しくは開設者に対して必要な報告をさせるとき、その理由を通知します(施行規則第114条)。
法第24条第1項及び第2項の規定により職員が立入検査等をするときは、当該職員はその身分を示す証明書を携帯し、関係者に提示します(法第24条第3項)。この身分を示す証明書は、様式第三十によるものです(施行規則第113条)。
認定再生医療等委員会との関係(施行規則第40条、第41条)
これまで見てきたように、再生医療等の提供には、再生医療等提供計画の審査、トラブル発生時の報告への対応、定期報告への対応、及びその他再生医療等の適正な提供のための対応等、認定再生医療等委員会の関与があり、再生医療等提供機関は、その医療活動のために、認定再生医療等委員会との関係を築く必要があります。そのための規定が施行規則第40条及び第41条に定められています。
認定再生医療等委員会に審査等業務を行わせるに際し、再生医療等を提供しようとする医療機関の管理者は、あらかじめ、次に掲げる事項を記載した文書により認定再生医療等委員会設置者(法第26条第5項第一号に規定する認定委員会設置者)との契約を締結しなければなりません(施行規則第40条)。ただし、この規定は、認定再生医療等委員会が、当該再生医療等を提供しようとする医療機関の開設者及び当該再生医療等を提供しようとする医療機関を有する法人が開設する/開設したものではない場合に適用されます。
認定再生医療等委員会設置者との契約書の記載事項(施行規則第40条)
- 当該契約を締結した年月日
- 再生医療等を提供しようとする医療機関及び当該認定再生医療等委員会の名称及び所在地
- 当該契約に係る業務の手順に関する事項
- 当該認定再生医療等委員会が意見を述べるべき期限
- 細胞提供者及び再生医療等を受ける者の秘密の保全に関する事項
- その他必要な事項
再生医療等を提供しようとする医療機関の管理者又は提供機関管理者は、認定再生医療等委員会から法第26条第1項各号に規定する意見を述べられた場合には、当該意見を受けて講じた再生医療等提供計画の変更その他の措置について、当該認定再生医療等委員会に対し報告を行います(施行規則第41条第1項)。この規定は、再生医療等を多施設共同研究として行う場合について準用します(施行規則第41条第2項)。
第三節のまとめ
ここまで、「第三節 再生医療等の適正な提供に関する措置」の規定を紹介しました。再生医療等を提供しようとする医療機関は、その医療機関の規則・細則の中にこれらの措置に対応する規定を設けて体制を整備します。
「第三章 認定再生医療等委員会」及び「第四章 特定細胞加工物の製造」において「認定再生医療等委員会」及び「特定細胞加工物製造事業者」を規定していますが、「第三章 認定再生医療等委員会」及び「第四章 特定細胞加工物の製造」は別の記事で紹介することとし、ここからは「第五章 雑則」及び「第六章 罰則」を紹介します。
第五章 雑則
再生医療等安全性確保法に規定する厚生労働大臣の権限は、厚生労働省令で定めるところにより、地方厚生局長に委任することができ、この規定により地方厚生局長に委任された権限は、厚生労働省令で定めるところにより、地方厚生支局長に委任することができます(法第56条)。
特定細胞加工物の製造に関する許可の更新を申請する者(病院外の国内事業者)及び特定細胞加工物の製造に関する認定の更新を申請する者(国外事業者)は、それぞれ当該各号の申請に対する審査に要する実費の額を考慮して政令で定める額の手数料を納めます(法第57条第1項)。
独立行政法人 医薬品医療機器総合機構(医薬品機構)が行う第38条第1項(第39条第2項において準用する場合を含む)に規定する細胞培養加工施設の構造設備の調査を受けようとする者は、当該調査に要する実費の額を考慮して政令で定める額の手数料を機構に納めます(法第57条第2項)。
第六章 罰則
再生医療等安全性確保法に規定する罰則
| 3年以下の拘禁刑若しくは300円以下の罰金 (法第59条) | 法第22条の規定による命令(緊急命令)に違反した者 |
| 1年以下の拘禁刑又は100万円以下の罰金 (法第60条) | 次の各号のいずれかに該当する者 一. 法第4条第1項の規定に違反して、第一種再生医療等提供計画を提出せず、又はこれに記載すべき事項を記載せず、若しくは虚偽の記載をしてこれを提出して、第一種再生医療等を提供した者 二. 法第5条第1項の規定に違反して、変更後の第一種再生医療等提供計画を提出せず、又はこれに記載すべき事項を記載せず、若しくは虚偽の記載をしてこれを提出して、第一種再生医療等を提供した者 三. 法第8条第1項(法第10条第1項において準用する場合を含む)の規定による命令に違反した者 四. 法第9条(法第10条第1項において準用する場合を含む)の規定に違反した者 五. 法第13条の規定に違反して第一種再生医療等を行った者 六. 法第23条第2項(第一種再生医療等に係る部分に限る)の規定による命令に違反した者 七. 法第29条の規定に違反して秘密を漏らした者 |
| 6月以下の拘禁刑又は30万円以下の罰金 (法第61条) | 次の各号のいずれかに該当する者 一. 法第35条第1項の規定に違反して許可を受けないで特定細胞加工物の製造をした者 二. 法第47条の規定による命令に違反した者 三. 法第48条第1項の規定による細胞培養加工施設の使用禁止の処分に違反した者(許可事業者に限る) 四. 法第48条第2項の規定による命令に違反した者(許可事業者に限る) 五. 法第49条の規定による命令に違反した者 |
| 50万円以下の罰金 (法第62条) | 次の各号のいずれかに該当する者 一. 法第4条第1項の規定に違反して、再生医療等提供計画を提出せず、又はこれに記載すべき事項を記載せず、若しくは虚偽の記載をしてこれを提出して、再生医療等を提供した者(法第60条第一号の規定に該当する者を除く) 二. 法第5条第1項の規定に違反して、変更後の再生医療等提供計画を提出せず、又はこれに記載すべき事項を記載せず、若しくは虚偽の記載をしてこれを提出して、再生医療等を提供した者(法第60条第二号の規定に該当する者を除く) 三. 法第13条の規定に違反して再生医療等を行った者(法第60条第五号の規定に該当する者を除く) 四. 法第16条第1項の規定に違反して記録を作成せず、又は虚偽の記録を作成した者 五. 法第16条第2項の規定に違反して記録を保存しなかった者 六. 法第23条第2項(第一種再生医療等に係る部分を除く)の規定による命令に違反した者 七. 法第24条第1項若しくは第2項の報告をせず、若しくは虚偽の報告をし、同条第1項若しくは第2項の規定による立入検査を拒み、妨げ、若しくは忌避し、又は同条第1項若しくは第2項の規定による質問に対し、正当な理由なしに答弁せず、若しくは虚偽の答弁をした者 |
| 20万円以下の罰金 (法第63条) | 次の各号のいずれかに該当する者 一. 法第40条第1項の規定に違反して、届出をしないで、又は虚偽の届出をして、特定細胞加工物の製造をした者 二. 法第48条第1項の規定による細胞培養加工施設の使用禁止の処分に違反した者(許可事業者を除く) 三. 法第48条第2項の規定による命令に違反した者(許可事業者を除く) 四. 法第51条の規定による命令に違反した者 五. 法第52条第1項若しくは第2項の報告をせず、若しくは虚偽の報告をし、同条第1項若しくは第2項の規定による立入検査(法第53条第1項の規定により機構が行うものを含む)を拒み、妨げ、若しくは忌避し、又は同条第1項若しくは第2項の規定による質問(法第53条第1項の規定により機構が行うものを含む)に対し、正当な理由なしに答弁せず、若しくは虚偽の答弁をした者 |
法人の代表者又は法人若しくは人の代理人、使用人その他の従業者が、その法人又は人の業務に関して法第59条、法第60条(第七号を除く)又は前三条の違反行為をしたときは、行為者を罰するほか、その法人又は人に対しても各本条の罰金刑を科す(法第64条)。
おわりに
ここまで、再生医療等提供機関に係る規定並びに雑則及び罰則を、再生医療等安全性確保法及び再生医療等安全性確保法施行規則から紹介しました。次の記事では、この記事では詳しく説明しなかった、認定再生医療等委員会を紹介します。




